太原市龙城智迅停车资源管理有限公司成立于2015年,是太原市龙城发展投资有限公司隶属的全资子公司,是经太原市政府授权,市城乡管理委员会委托,也是太原市政府唯一授权的国有停车资源管理公司。为满足新开场站人员需求,现需启动招聘及储备劳务用工工作,面向社会招聘工作人员。
一、招聘岗位与职责: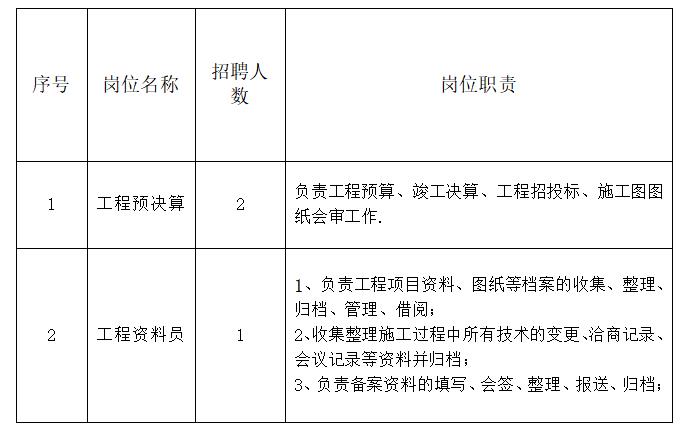 二、报名资格条件:
二、报名资格条件:认同公司的发展目标、经营理念及企业文化,具有较强的事业心、责任感,具有良好的团队合作与无私奉献精神;具有良好的政治思想素质和职业道德操守,勤奋敬业、遵纪守法、品行端正、无违规违法等不良记录。
(一)工程预决算:1.岗位条件:(1)大学本科及以上学历,土建、电气安装、工程造价等相关专业;(2)年龄在35周岁以下;(3)具有中级工程师及注册造价工程师证书;(4)工作认真、严谨,具有吃苦耐劳精神。2.薪资待遇:5000元/月。(二)工程资料员:1.岗位条件:(1)大学本科及以上学历,工程类相关专业;(2)年龄在40周岁以下;(3)同等条件下,具有2年及以上相关工作经验者优先;(4)工作认真、严谨,具有吃苦耐劳精神。2.薪资待遇:5000元/月。三、报名流程:(一)报名:1、报名方式:登录“太原青创”网站(http://www.tyqc.com.cn),首页点击“考试报名”进入网上报名系统,或搜索“太原青创人力资源”公众号,左下角点击“考试报名”进入网上报名系统,仔细阅读报名须知,按照报考流程注册账号并登录系统选择报考岗位进行填报。报考人员只能选择一个招聘岗位进行报名。2、报名时需要上传以下资料:(1)本人二代身份证原件(正反面);(2)户口簿原件(首页及本人页);(3)近期一寸红底免冠照电子版;(4)毕业证书原件;(5)学信网下载《教育部学历证书电子注册备案表》;(6)职称、资格证书原件;(7)原单位出具的工作证明原件(工作证明中需加盖原单位公章,注明从事的岗位及年限);(8)本人户籍地派出所三个月内开具的《无犯罪记录证明》原件。(二)资格审查:1、报考人员须对报名材料的真实性负责。根据要求对应聘人员进行严格的资格审查,考生资料审查贯穿整个招聘过程中,报名人员对所提供的材料负诚信责任,凡提供虚假材料的,一经查实,取消应聘资格。2、报考人员认真填写报名信息并将报名所需资料证件、证书原件拍照上传,上传资料要求清晰完整,等待审核通过后缴纳报名考试费。(三)报名缴费:报名费 10元/人。(四)考核:报名结束后,由太原市龙城智迅停车资源管理有限公司组织面试考核。(五)体检:面试合格后由太原青创人力资源有限公司统一安排体检。四、人事管理:(一)用工形式:录用人员与太原青创人力资源有限公司签订劳动合同,由太原青创人力资源有限公司派至太原龙城智迅停车资源管理有限公司工作。(二)合同期限:首次签订期限为两年,试用期为两个月,到期后视情况续签。五、工作地址:主要以南内环以南。六、联系电话:0351-3090226 ??范老师。七、温馨提示:太原市龙城智迅停车资源管理有限公司、太原青创人力资源有限公司未委托任何个人进行招聘,且不收取报名者任何费用,希望广大求职者提高警惕,谨防上当受骗。
【太原临床志愿者 · 5月招募】男女不限48+40人,营养补助6天6000元 ▍太原招聘



也可以手动填写发给我们
报名人
姓名:
性别:
年龄:
身高:? CM
体重:? KG(不要填斤,是公斤=斤/2)
身份证号:
联系电话:
项目医院:山西省人民医院
项目价格:6000元
项目药名:氨氯地平贝那普利片-口服
现居住地:
山西省人民医院召开Ⅰ期临床试验研究室揭牌仪式暨仿制药
一致性评价工作启动会
? ? ?2017年9月29日,山西省人民医院召开Ⅰ期临床试验研究室揭牌仪式暨仿制药一致性评价工作启动会,省食品卫生食药局领导和省卫生计生委相关领导参加了此次会议。
? ? ?李荣山院长表示,要积极响应国家推动医药创新发展的号召,做好仿制药一致性评价工作。(山西省人民医院供稿)
一图带你了解“药物临床试验”
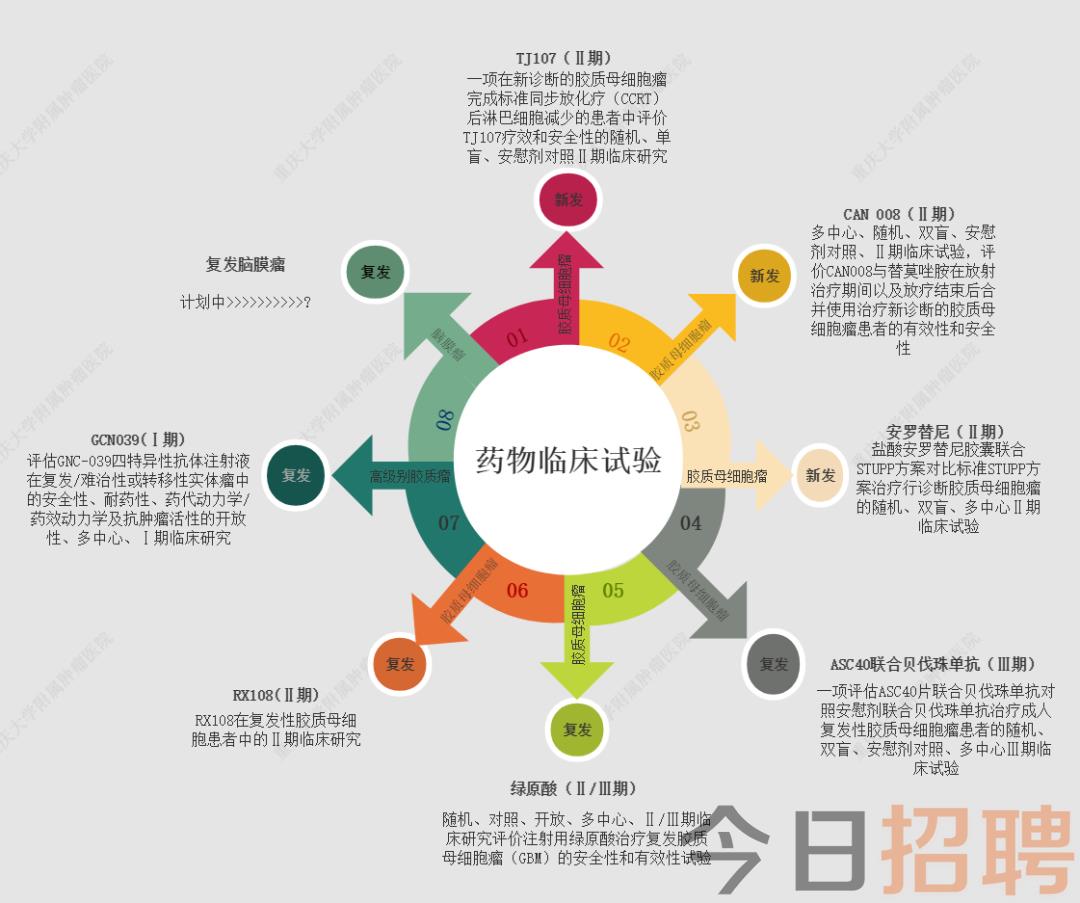
图1:重庆大学附属肿瘤医院神经外科药物临床试验研究现状
? ? ?重庆大学附属肿瘤医院神经外科持续开展药物临床试验研究,目前我科在研临床试验项目共7项,计划中1项(图1)。
什么是临床试验?
图 2药物临床试验
临床试验(ClinicalTrial),指任何在人体(病人或健康志愿者)进行药物的系统性研究,以证实或揭示试验药物的作用、不良反应及试验药物的吸收、分布、代谢和排泄,目的是确定试验药物的疗效与安全性。
www.clinicaltrail.gov,截止2021年在此官网上登记的针对脑胶质瘤的临床研究多达1000多项,并且多以药物治疗为主。而就国内而言,目前中国临床试验注册中心平台上的注册临床实验共计50余项,且在逐年递增中。
如何进行临床试验?

临床试验需要合适的患者在合适的时机参加,两个合适同时满足才有可能参加到临床试验中,因为所有的受试者完整试验过程必要经过知情同意期——筛选期——治疗期——随访期。
知情同意期:该阶段主要是受试者与临床试验团队充分沟通阶段,所有的参与临床试验的前提是患者充分知情且完全自愿参加,即受试者必要在充分知情的情况下自愿参加临床试验项目的,同时患者有权随时退出临床试验;
筛选期:该阶段主要完成必要检查、检验及病史资料收集汇总等,同时临床试验方案对受试者都有明确的限定,即入选标准和排除标准,只有完全符合入选标准且不符合排除标准的患者才能进入后续的治疗期;
治疗期:正式进入后续治疗中,按照试验方案给予药物治疗和随访,完成药物的使用和使用前后的情况评估,包括安全性与疗效的综合评估。
随访期:治疗结束或提前退出后进入后续随访期。常以电话访视进行,也可现场访视,持续关注受试者治疗结束或终止后的后续情况。



 太原
太原


